Kernaussagen:
– Vorläufige Daten von Pfizer und BioNTech zeigten, dass ihr COVID-19-Impfstoff bei der Prävention der Krankheitssymptome zu mehr als 90 % wirksam war, verglichen mit den allgemeinen Erwartungen von 60% bis 70%.
– Die Aktienmärkte schnellten nach Bekanntgabe der Untersuchungsergebnisse in die Höhe: Der Dow Jones Industrial Average und der S&P 500® Index verzeichneten während des Intraday-Handels Höchststände.
– Obwohl es bei der Wirksamkeit des Impfstoffs zur Bekämpfung der globalen Pandemie noch viele Unsicherheiten gibt, waren die ersten Ergebnisse sehr ermutigend und wecken neuen Optimismus hinsichtlich einer Belebung des Wirtschaftswachstums im Jahr 2021.
In dieser Woche – weniger als ein Jahr nach dem ersten Auftreten des Corona-Virus – gaben die Biopharmaunternehmen Pfizer und BioNTech bekannt, dass ihr neuartiger Impfstoff gegen COVID-19 in einer fortgeschrittenen klinischen Studie die tödliche Krankheit zu über 90 % verhindern konnte. Obwohl es sich um vorläufige Daten handelt, waren die Ergebnisse besser als erwartet und entfachen neuen Optimismus hinsichtlich des Wirtschaftswachstums im Jahr 2021 – eine Einschätzung, die wir zunehmend teilen.
Die Bedeutung von 90 Prozent
Dies ist die erste Datenauswertung von fast einem Dutzend groß angelegter klinischer Studien für COVID-19-Impfstoffe. Um es einfach auszudrücken, das Ergebnis war höchst ermutigend. Die Konsenserwartungen hatten die Wirksamkeit des derzeit als BNT162b2 bekannten Impfstoffs auf 60 % bis 70 % prognostiziert. Sollte die Wirksamkeitsrate von 90 % bis zum Ende der Studie bestehen bleiben, wäre die Wirksamkeit des Medikaments gleichwertig mit der des Masernimpfstoffs und deutlich höher als bei einer Grippeimpfung (durchschnittlich 50 % wirksam). Obwohl keine Sicherheitsdaten zur Verfügung gestellt wurden, erklärte Pfizer außerdem, dass unter den mehr als 43.500 Personen, die derzeit an der weltweiten Studie teilnehmen, bisher keine ernsthaften Nebenwirkungen beobachtet wurden.
Was kommt als nächstes?
Sicherlich können sich diese Werte ändern, wenn mehr Daten eintreffen. Die Ergebnisse basieren auf 94 Patienten mit bestätigten Symptomen von COVID-19. (Die Patienten erhielten über drei Wochen zwei Dosen entweder des Impfstoffs oder eines Placebos, wobei der Schutz 28 Tage nach der ersten Dosis erreicht wurde). Nach Angaben der Unternehmen wird die Studie fortgesetzt, bis 164 Fälle vorliegen. In der Zwischenzeit können Pfizer und BioNTech bei der US-Arzneimittelbehörde FDA (Food and Drug Administration) eine Genehmigung für die Notfallverwendung beantragen, nachdem sie im Durchschnitt zwei Monate lang Arzneimittelsicherheitsdaten gesammelt haben – ein Ziel, das planmäßig bis zur dritten Novemberwoche erreicht werden soll. Da die FDA von einem Impfstoff eine Wirksamkeit von mindestens 50% erwartet, glauben wir, dass Pfizer und BioNTech sich jetzt einen ausreichenden Spielraum für eine mögliche Zulassung verschafft haben.
Ein guter Tag für Biopharma-Innovation, Kooperation und Zusammenarbeit
BNT162b2 basiert auf einem neuartigen Ansatz zur Medikamentenentwicklung, der so genannten Messenger-Ribonukleinsäure (mRNA)-Technologie, die den Körper im Wesentlichen veranlasst, Proteine zur Bekämpfung von Krankheiten herzustellen. Im Fall von COVID-19 trägt BNT162b2 die Baupläne für den Aufbau einer Proteinsäule, mit der SARS-CoV-2 (das Virus, das COVID-19 verursacht) in die Wirtszellen eindringt und eine Reaktion des Immunsystems auslöst. Bislang wurden noch keine mRNA-basierten Therapien, auch nicht für andere Krankheiten wie Krebs, zugelassen. Sollte die Arbeit von Pfizer und BioNTech erfolgreich sein, wäre es nicht nur wegen des Nachweises, dass die Technologie funktioniert, sondern auch im Hinblick auf den Zeitplan bemerkenswert: BNT162b2 wird in weniger als einem Jahr für den Notfalleinsatz entwickelt und zugelassen worden sein, während es in der Vergangenheit zehn Jahre oder länger gedauert hat, bis Impfstoffe auf den Markt kamen.
Zudem war die Entwicklung des Medikaments das Ergebnis einer außergewöhnlichen Zusammenarbeit. BioNTech, ein deutsches Biotech-Unternehmen, entwarf die Struktur des Medikaments, verfügte aber nicht über die Ressourcen, um eine weltweite klinische Studie durchzuführen. Daher wandte sich BioNTech Anfang dieses Jahres an den Pharmariesen Pfizer, der sich bereit erklärte, bei der Entwicklung des Medikaments zu helfen. Entscheidend war, dass Pfizer auch den Ausbau der Fertigungs- und Vertriebskapazitäten vorangetrieben hat. Die mRNA-Therapie stellt eine besondere Herausforderung dar, da sie bei extrem niedrigen Temperaturen transportiert und gelagert werden muss, um wirksam zu bleiben. Pfizer investierte Milliarden von Dollar in die Entwicklung von Versandbehältern mit wiederverwendbaren GPS-Temperatursensoren und speziellen Gefrierschränken, in denen die Fläschchen bis zu sechs Monate lang aufbewahrt werden können. Auf der Grundlage aktueller Prognosen sind Pfizer und BioNTech daher auf dem besten Weg, bis Ende 2020 50 Millionen Dosen (für 25 Millionen Menschen) und bis 2021 bis zu 1,3 Milliarden Dosen (für 650 Millionen Menschen) herzustellen – eine weitere bemerkenswerte Leistung.
Ein neuer Tag für globale Märkte
Bei der Wirksamkeit des Impfstoffs zur Bekämpfung der globalen Pandemie gibt es noch viele Unsicherheiten. Die FDA muss zum einen sicherstellen, dass Pfizer und BioNTech Impfstoffdosen sicher und konstant herstellen können. Es sind weitere Untersuchungen erforderlich, um die Wirksamkeit und Beständigkeit der Behandlung, insbesondere bei verschiedenen Altersgruppen, zu bestätigen und um festzustellen, ob die Impfung schwere Infektionen verhindert und spätere Krankenhausaufenthalte und Todesfälle reduziert. Eine Genehmigung für den Notfalleinsatz würde es ermöglichen, den Impfstoff zunächst an gefährdete Bevölkerungsgruppen zu verabreichen, z. B. an Mitarbeiter des Gesundheitswesens an vorderster Front. Allerdings beginnen die frühesten Impfungen voraussichtlich erst Ende des Jahres.
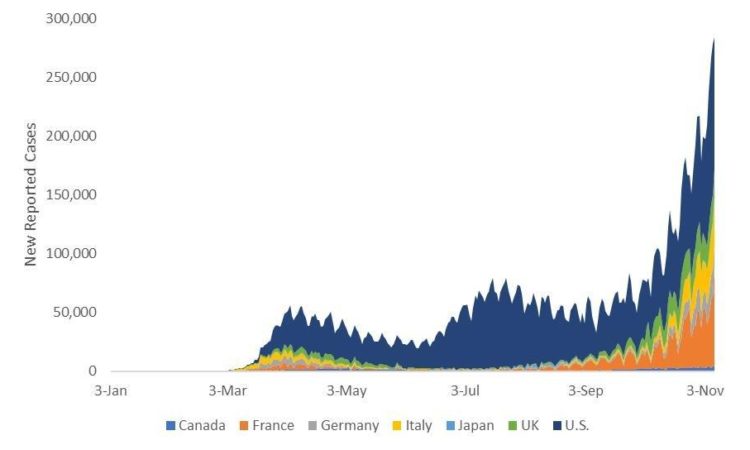
COVID-19-Fälle steigen sprunghaft
Die positiven Nachrichten über einen Impfstoff kommen zu einem entscheidenden Zeitpunkt, da weltweit mehr als 50 Millionen Fälle bestätigt wurden und die Zahl der neuen Fälle in den G7-Ländern rapide zunimmt.
Dennoch stiegen die Aktienmärkte nach Bekanntgabe der Untersuchungsergebnisse sprunghaft an: Der Dow Jones Industrial Average und der S&P 500® Index erreichten Höchststände, vor allem bei den Branchen, die von der Pandemie am stärksten betroffen waren, wie die Reise- und Energiebranche. In der Tat haben sich in den letzten 48 Stunden die Prognosen für Risikoanlagen deutlich positiver entwickelt, was nicht nur den Impfstoffnachrichten zu verdanken ist, sondern auch dem Ende der US-Präsidentschaftswahlen (mit dem Potenzial, dass eine gespaltene US-Regierung zu moderaten politischen Veränderungen führen könnte). Beide Ereignisse könnten im Jahr 2021 zu einem verbesserten Wirtschaftswachstum, der Rückkehr des Anlegervertrauens und positiven Nettoflüssen in Risikoanlagen führen.
Wichtig ist, dass dies auch zu einer Ausweitung der Marktgewinne führen könnte. Während des gesamten Jahres 2020 konzentrierte sich die Outperformance weitgehend auf Unternehmen mit hohen Wachstumsraten, die digitale Lösungen für eine Welt anboten, in der Social Distancing die neue Normalität darstellte. Sollte ein Impfstoff dazu beitragen, die „alte Normalität“ in der Weltwirtschaft wiederherzustellen, erwarten wir, dass sich diese Begrenzung endlich ausweitet.
Volatilität ist nicht ausgeschlossen, vor allem, wenn demnächst weitere Volkswirtschaften in den Lockdown gehen, während wir auf die weltweite Verteilung eines Impfstoffs warten. Aber die Nachrichten von Pfizer und BioNTech lassen hoffen, dass eine Lösung in Sicht ist und dass andere Impfstoffe, die auf dasselbe SARS-CoV-2-Protein abzielen – darunter eine zweite mRNA-Therapie aus Moderna – erfolgreich sein könnten. Die Zulassung mehrerer Impfstoffe wird als entscheidend für einen raschen und wirksamen Schutz der Weltbevölkerung angesehen, mit erheblichen Auswirkungen auf die Weltwirtschaft. Darüber hinaus könnten mRNA-Plattformen von Natur aus leicht angepasst werden, um neue Virusformen zukünftig zu bekämpfen, sollte dies notwendig werden.
Der typische Marktzyklus (von der Baisse bis zur Hausse) dauert etwa fünf Jahre. Die COVID-19-Pandemie hat dem letzten Bullenmarkt im März ein abruptes Ende bereitet. Die Nachrichten dieser Woche könnten einen wichtigen Punkt auf dem Weg zu einem neuen markieren.
Dieser Kommentar ist ausschließlich für den Gebrauch von Medienvertretern bestimmt und sollte nicht von Privatanlegern, Finanzberatern oder institutionellen Investoren verwendet werden. Wir können Telefonanrufe zur wechselseitigen Absicherung, zur Verbesserung des Kundenservice und zwecks regulatorisch erforderlicher Aufzeichnungen speichern.
Janus Henderson Group (JHG) ist ein weltweit führender aktiver Vermögensverwalter, der seine Aufgabe darin sieht, Anleger beim Erreichen ihrer langfristigen finanziellen Ziele zu unterstützen. Dazu wird ein breites Spektrum von Lösungen angeboten, wie Aktien-, Anleihen-, quantitative Aktien-, Multi-Asset- und alternative Strategien.
Janus Henderson verwaltet ein Anlagevermögen von etwa EUR 299,8 Milliarden (Stand: 30. Juni 2020) und hat über 2.000 Mitarbeiter sowie Büros in 28 Städten weltweit. Das Unternehmen mit Sitz in London ist an der New York Stock Exchange (NYSE) und der Australian Securities Exchange (ASX) notiert.
Janus Henderson Investoren
Tower 185, 25th floor, Friedrich-Ebert-Anlage 35-37
60327 Frankfurt am Main
Telefon: +49 (69) 86003-0
Telefax: +49 (69) 86003-355
http://www.henderson.com
Dolphinvest Communications Limited
Telefon: +49 (69) 339978-17
E-Mail: stschorn@dolphinvest.eu
Dolphinvest Communications Limited
Telefon: +49 (69) 339978-11
E-Mail: mmossdorf@dolphinvest.eu
![]()